UNIDAD 3. Ciencias Naturales. Cambios en la estructura de la Materia. 2º ESO.
Tema 3: Cambios en la estructura de la materia.
1. Cambios térmicos:
Cambios térmicos en la materia
Las atracciones intermoleculares: Las moléculas se atraen entre sí con fuerzas electromagnéticas de corto alcance, llamadas fuerzas de cohesión.
La agitación térmica: Todas las partículas vibran o se desplazan con velocidades altísimas. Las moléculas que forman el aire se desplazan a unos 1600 km/h .
Los estados de agregación
Sólido: a bajas temperaturas, las fuerzas eléctricas de cohesión predominan y las partículas se unen y forman aglomerados sólidos.
Líquidos: en los líquidos encontramos una estructura muy caótica de la materia, donde coexisten pequeños gránulos que conservan aún la forma cristalina con partículas liberadas que se desplazan y chocan unas con otras.
Gaseoso: la materia en estado gaseoso se encuentra en un desorden absoluto. Las partículas, muy lejanas unas de otras para que actúen las fuerzas de cohesión, se mueven a altísimas velocidades con m.r.u. hasta que encuentran algo con qué chocar.
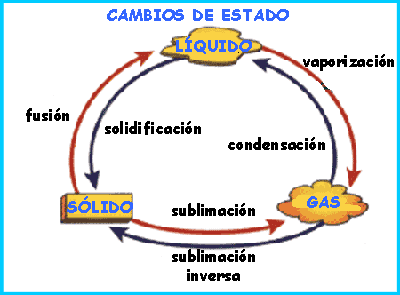
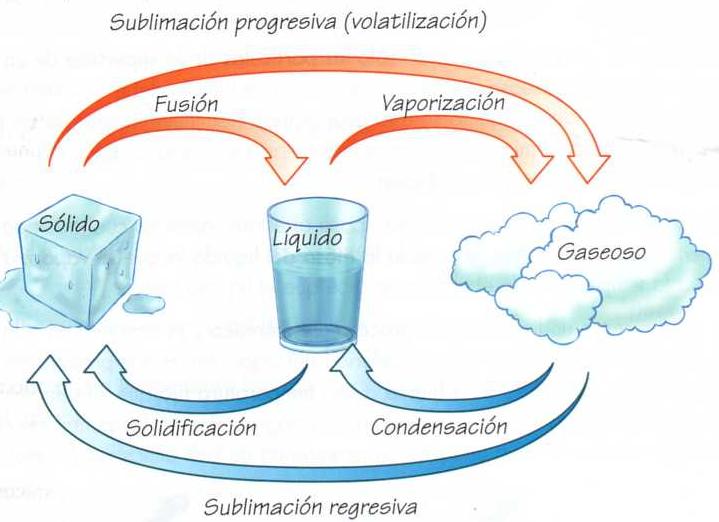
Los cambios de estado
Fusión: si a un sólido le suministramos suficiente energía térmica, la vibración de sus partículas aumenta, y la estructura ordenada se derrumba.
Vaporización:si seguimos suministrando energía térmica, la agitación es tan fuerte que las partículas rompen sus fuerzas atractivas y escapan del líquido.
2. Cambios químicos
Las uniones de los átomos que forman la materia
Si se exceptúan los elementos inertes, los átomos tienden a unirse mediante intensas fuerzas electromagnéticas para formar moléculas o cristales. Son los cambios químicos, en los que se intercambian grandes cantidades de energía
La sustancias atómicas o gases inertes
El Helio (He), el neón (Ne), el argón (Ar), el kriptón (kr), etc., están formados por átomos libres.
Las sustancias moleculares
Están formadas por moléculas, que son partículas con un número fijo de átomos. Así, el nitrógeno del aire (dinitrógeno) está formado por moléculas de dos átomos de nitrógeno.
Las sustancias cristalinas
Están formadas por cristales, partículas constituidas por átomos perfectamente ordenados en estructuras geométricas con un número indeterminado de ellos.
3. Otros conceptos químicos importantes
Los elementos
Elementos son aquellas sustancias que están formadas por átomos de la misma clase.
Elementos formados por átomos aislados
Estos átomos se encuentran muy separados unos de otros; es el caso de los gases inertes, como el helio (He), el neón (Ne) , el argón (Ar), que podemos encontrar el aire.
Elementos formados por moléculas
Están formados por moléculas constituidas por dos o tres átomos iguales; por ejemplo, el oxígeno (o2), el ozono(o3), el hidrógeno (H2), etc.
Elementos que forman cristales
Ya hemos estudiado que los cristales son grandes estructuras ordenadas con todos sus átomos iguales. Así se encuentran metales como el hierro (Fe), la plata (Ag), o el estaño (Sn).
Los compuestos
Cuando las partículas que constituyen una sustancia están formadas por átomos de diferentes clases, esa sustancia es un compuesto.
Compuestos moleculares
Ya hemos visto que están formados por moléculas; es el caso del agua, (H2O), o el ácido sulfúrico, H2SO4
Compuestos cristalinos
Es el caso de la sal común, NaCI, Formada por cristales que contienen el mismo número de átomos de sodio que de cloro, o el sulfato cúprico.
Diversidad de los compuestos químicos
Si miras a tu alrededor podrás contemplar, de una sola ojeada, decenas de sustancias distintas. Hoy conocemos millones de compuestos químicos.
-Los compuestos orgánicos: Son los que siempre tienen en su molécula átomos de carbono, combinados, fundamentalmente, con hidrógeno, oxígeno y nitrógeno; son las sustancias que producen los seres vivos
Los compuestos inorgánicos: Son los que forman los minerales y las rocas, algunos gases del aire como el CO2, y el agua (H2O). Son los que constituyen la Luna y los demás planetas.
4. Ecuaciones químicas
Los símbolos de los elementos
En una ecuación química, a los elementos (sustancias formadas por átomos iguales ) se les representa por un símbolo. Así, el hierro es Fe; el carbono, C; el níquel, Ni; etc.
Formulas de los compuestos
Los compuestos ( sustancias cuyas moléculas o cristales están formadas por átomos diferentes) se representa mediante fórmulas.
Reactivos y productos
A las sustancias que entran en reacción se les llama reactivos, sean estas elementos o compuestos, y a las que se forman en ella, productos de reacción.
0 comentarios